



蛋白类药物在生物医药中占据着举足轻重的地位🌿。2018年全球医药销售额前十的药物中🧞♂️,七种为蛋白质药物🚶♂️。蛋白质自身很难跨越细胞膜,因此🧜🏼♂️👩👩👧👧,当前蛋白类药物都是基于胞外靶点开发的✅。然而胞外蛋白质在人类基因组编码的蛋白质当中仅占不到30%👩🦯,这一局限性制约了蛋白类药物的发展。开发高效、安全的蛋白质胞内递送技术对于生物医药🛀🏼、生命科学基础研究都具有重要的意义。
现有蛋白质胞内递送载体通常需要对蛋白质进行化学修饰或基因工程改造来帮助其结合蛋白质。这一策略不仅涉及复杂的化学或生物合成🖐🏽,而且可能会导致修饰后的蛋白质结构或生物学功能发生不可逆的改变。近期,天美娱乐程义云团队发现富含硼酸的高分子可以有效解决上述问题,在不需要修饰的条件下,对多种蛋白质实现了高效🛌🏿、普适的蛋白质胞内递送,并能维持这些蛋白质的生物活性。这一成果近日发表于Science Advances (2019, 5, eaaw8922)。

蛋白质表面同时存在大量的阴离子氨基酸(谷氨酸、天冬氨酸)和阳离子氨基酸(赖氨酸🤬、精氨酸👩🏻💼、组氨酸)🍚,阳离子高分子可以通过静电相互作用结合蛋白质表面的阴离子基团,但是残留的阳离子氨基酸则会和高分子链产生排斥,从而影响蛋白质复合物的稳定性。如果设计一种能够同时结合阴离子和阳离子基团的载体,则可以有效解决上述问题🏊🏼。基于上述考虑,程义云团队设计了一种富含苯硼酸的阳离子高分子。苯硼酸是一种缺电子基团,可以通过氮-硼配位与蛋白质表面的氨基🤦🏽♂️、咪唑等结合👩🏼🍳,阳离子高分子上的氨基可以与蛋白质表面的羧基结合🧣,进而形成稳定的复合物(图1)🧑🏻🦰。这种方式使得富含硼酸的高分子能够结合不同等电点、尺寸的蛋白质分子🧑🏻🦰,实现普适的蛋白质胞内递送🧑🏿💼。这种高分子可以将牛血清白蛋白➡️、藻红蛋白、绿色荧光蛋白、红色荧光蛋白、黄色荧光蛋白🆓、细胞色素c、溶菌酶🧘🏻♂️、胰蛋白酶、β-半乳糖苷酶、皂角素、核酸酶、核糖核蛋白等十余种蛋白质高效递送到细胞质中(图2),且能够很好地维持这些蛋白质的生物活性(图3)。进一步,程义云团队和浙江大学平渊教授合作,评估了这种高分子载体向多种细胞中递送Cas9核糖核蛋白的效率,发现其可以实现高效的CRISPR/Cas9基因编辑。这种高分子具有非常高的商业应用价值,是一种通用型蛋白质胞内递送载体🌠,目前该团队正在推进该材料的商业化应用。
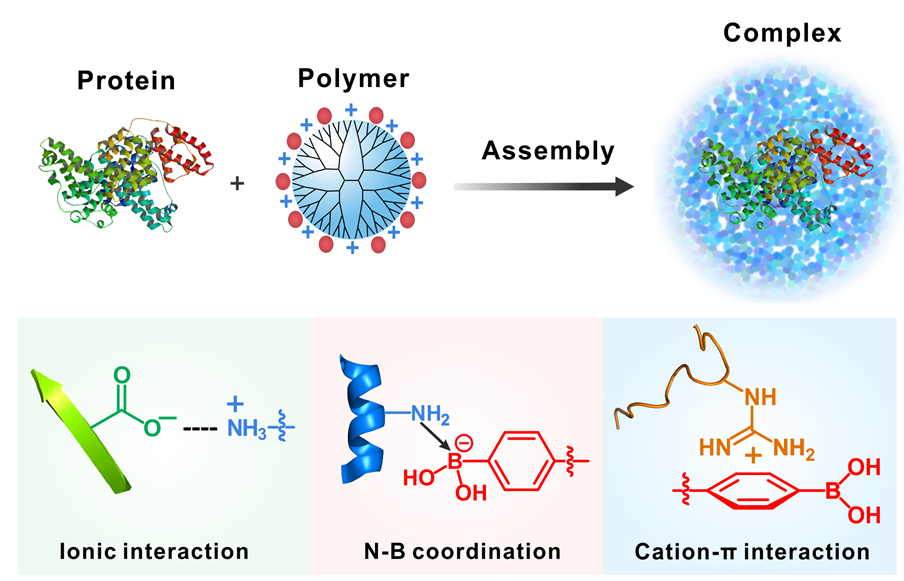
图1. 富含硼酸的阳离子高分子可以通过多种相互作用结合蛋白质。
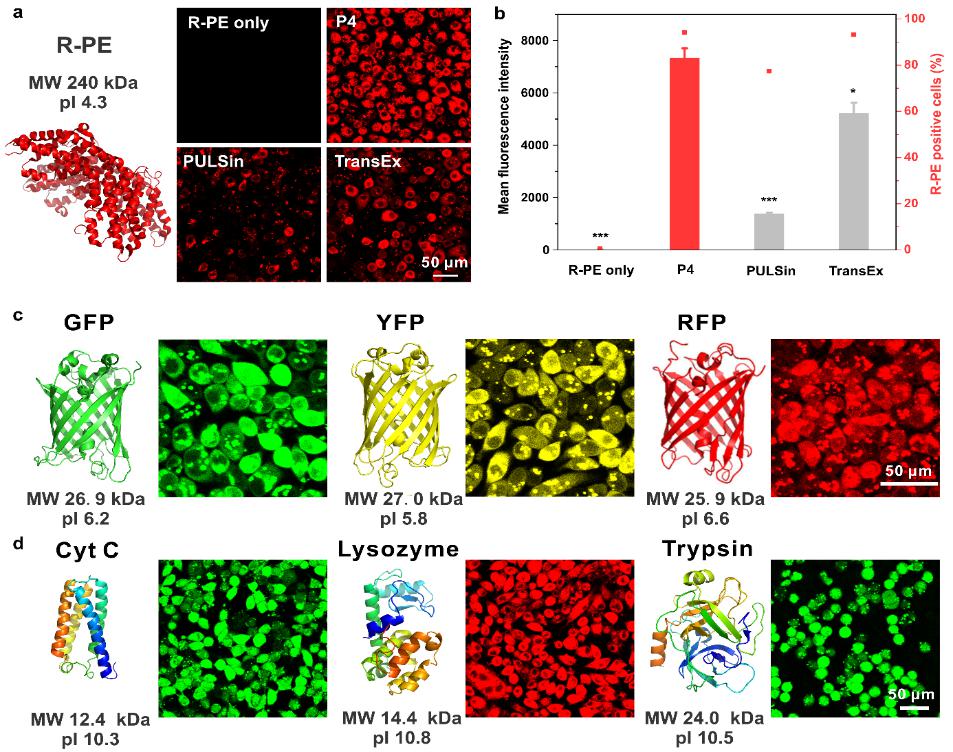
图2.富含硼酸的高分子可以高效递送不同分子量☝🏽、等电点的蛋白质。
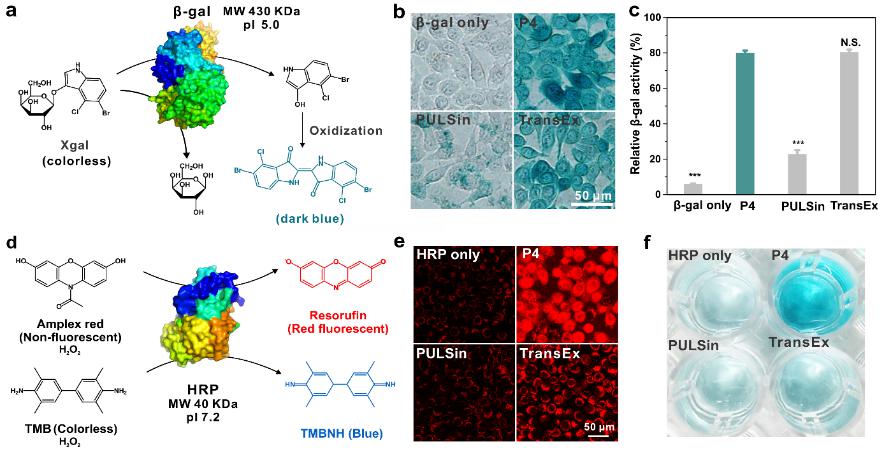
图3. 富含硼酸的高分子可以递送不同的蛋白酶,并维持这些酶的生物活性。
该论文的第一作者为天美娱乐博士生刘崇懿和浙江大学博士生万涛👩🏻💼,通讯作者为程义云教授和浙江大学平渊教授。天美为该论文的第一单位🙎🏿。该研究得到了国家自然科学基金杰出青年基金、上海市优秀学术带头人等项目的经费支持。
论文链接:https://advances.sciencemag.org/content/advances/5/6/eaaw8922.full.pdf